في مجال الطب الحديث، أثبتت المضادات الحيوية أنها من أهم الإنجازات، إذ ساهمت بشكل كبير في خفض معدلات الإصابة والوفيات المرتبطة بالعدوى الميكروبية. وقد أدى تأثيرها على تحسين نتائج العلاج السريري للعدوى البكتيرية إلى زيادة متوسط عمر المرضى. تُعد المضادات الحيوية ضرورية في الإجراءات الطبية المعقدة، بما في ذلك العمليات الجراحية، وزراعة الأعضاء، وزراعة الأعضاء، والعلاج الكيميائي. مع ذلك، يُشكل ظهور مسببات الأمراض المقاومة للمضادات الحيوية مصدر قلق متزايد، مما يُقلل من فعالية هذه الأدوية بمرور الوقت. وقد تم توثيق حالات مقاومة المضادات الحيوية في جميع فئات المضادات الحيوية نتيجةً لحدوث طفرات ميكروبية. وقد ساهم الضغط الانتقائي الذي تُمارسه الأدوية المضادة للميكروبات في ظهور سلالات مقاومة، مما يُشكل تحديًا كبيرًا للصحة العالمية.
لمواجهة مشكلة مقاومة المضادات الحيوية المُلحة، من الضروري تطبيق سياسات فعّالة لمكافحة العدوى تحدّ من انتشار مسببات الأمراض المقاومة، إلى جانب تقليل استخدام المضادات الحيوية. علاوة على ذلك، ثمة حاجة ماسة إلى أساليب علاجية بديلة. وقد برز العلاج بالأكسجين عالي الضغط كطريقة واعدة في هذا السياق، حيث يتضمن استنشاق أكسجين نقي بنسبة 100% عند مستويات ضغط محددة لفترة زمنية معينة. وباعتباره علاجًا أساسيًا أو مكملاً للعدوى، قد يُقدّم العلاج بالأكسجين عالي الضغط أملًا جديدًا في علاج العدوى الحادة التي تُسببها مسببات الأمراض المقاومة للمضادات الحيوية.
يُستخدم هذا العلاج بشكل متزايد كعلاج أساسي أو بديل لحالات مرضية متنوعة، تشمل الالتهابات، والتسمم بأول أكسيد الكربون، والجروح المزمنة، وأمراض نقص التروية، والعدوى. وتُعدّ التطبيقات السريرية للعلاج بالأكسجين عالي الضغط في علاج العدوى بالغة الأهمية، إذ تُوفّر فوائد قيّمة للمرضى.

التطبيقات السريرية للعلاج بالأكسجين عالي الضغط في علاج العدوى
تدعم الأدلة الحالية بقوة استخدام العلاج بالأكسجين عالي الضغط، سواءً كعلاج مستقل أو كعلاج مساعد، لما له من فوائد كبيرة للمرضى المصابين بالعدوى. خلال العلاج بالأكسجين عالي الضغط، يمكن أن يرتفع ضغط الأكسجين في الدم الشرياني إلى 2000 ملم زئبق، ويمكن أن يؤدي تدرج ضغط الأكسجين العالي الناتج بين الأكسجين والأنسجة إلى رفع مستويات الأكسجين في الأنسجة إلى 500 ملم زئبق. تُعد هذه التأثيرات ذات قيمة خاصة في تعزيز التئام الاستجابات الالتهابية واضطرابات الدورة الدموية الدقيقة التي تُلاحظ في البيئات الإقفارية، وكذلك في علاج متلازمة الحيز.
يمكن أن يؤثر العلاج بالأكسجين عالي الضغط أيضًا على الحالات المرضية التي تعتمد على الجهاز المناعي. تشير الأبحاث إلى أن هذا العلاج قد يثبط متلازمات المناعة الذاتية والاستجابات المناعية الناتجة عن المستضدات، مما يساعد على الحفاظ على تقبل الجسم للأعضاء المزروعة عن طريق تقليل دوران الخلايا الليمفاوية وكريات الدم البيضاء مع تعديل الاستجابات المناعية. بالإضافة إلى ذلك، فإن العلاج بالأكسجين عالي الضغطيدعم الشفاءيُعالج هذا العلاج الآفات الجلدية المزمنة عن طريق تحفيز تكوين الأوعية الدموية، وهي عملية حيوية لتحسين الشفاء. كما يُشجع هذا العلاج على تكوين مصفوفة الكولاجين، وهي مرحلة أساسية في التئام الجروح.
يجب إيلاء عناية خاصة لبعض أنواع العدوى، لا سيما العدوى العميقة والتي يصعب علاجها، مثل التهاب اللفافة الناخر، والتهاب العظم والنقي، والتهابات الأنسجة الرخوة المزمنة، والتهاب الشغاف المعدي. ومن أكثر التطبيقات السريرية شيوعًا للعلاج بالأكسجين عالي الضغط علاج التهابات الجلد والأنسجة الرخوة والتهاب العظم والنقي المصاحب لانخفاض مستويات الأكسجين، والذي غالبًا ما يكون سببه البكتيريا اللاهوائية أو المقاومة للمضادات الحيوية.
1. التهابات القدم السكرية
قدم السكريتُعدّ القرح من المضاعفات الشائعة لدى مرضى السكري، إذ تُصيب ما يصل إلى 25% منهم. وتنشأ العدوى بشكل متكرر في هذه القرح (حيث تُمثّل 40-80% من الحالات)، مما يؤدي إلى زيادة معدلات الاعتلال والوفيات. وتتكوّن عدوى القدم السكرية عادةً من عدوى متعددة الميكروبات، مع تحديد مجموعة متنوعة من مسببات الأمراض البكتيرية اللاهوائية. ويمكن لعوامل مختلفة، بما في ذلك عيوب وظائف الخلايا الليفية، ومشاكل تكوين الكولاجين، وآليات المناعة الخلوية، ووظائف الخلايا البلعمية، أن تُعيق التئام الجروح لدى مرضى السكري. وقد حدّدت العديد من الدراسات ضعف أكسجة الجلد كعامل خطر قوي للبتر المرتبط بعدوى القدم السكرية.
كأحد الخيارات الحالية لعلاج عدوى القدم السكريةأُفيد بأن العلاج بالأكسجين عالي الضغط يُحسّن بشكل ملحوظ معدلات التئام قرح القدم السكرية، مما يقلل الحاجة إلى البتر والتدخلات الجراحية المعقدة. فهو لا يقلل فقط من الحاجة إلى الإجراءات المكلفة، مثل جراحات ترقيع الجلد، بل يتميز أيضًا بانخفاض تكلفته وقلة آثاره الجانبية مقارنةً بالخيارات الجراحية. وقد أظهرت دراسة أجراها تشين وآخرون أن أكثر من 10 جلسات من العلاج بالأكسجين عالي الضغط أدت إلى تحسن بنسبة 78.3% في معدلات التئام الجروح لدى مرضى السكري.
2. التهابات الأنسجة الرخوة النخرية
تُعدّ التهابات الأنسجة الرخوة النخرية (NSTIs) في كثير من الأحيان متعددة الميكروبات، وتنشأ عادةً من مزيج من مسببات الأمراض البكتيرية الهوائية واللاهوائية، وغالبًا ما تترافق مع إنتاج الغازات. ورغم ندرة هذه الالتهابات نسبيًا، إلا أنها تُسبب معدل وفيات مرتفعًا نظرًا لتطورها السريع. ويُعدّ التشخيص والعلاج المناسبان في الوقت المناسب عنصرين أساسيين لتحقيق نتائج إيجابية، وقد تم التوصية بالعلاج بالأكسجين عالي الضغط (HBOT) كطريقة مساعدة في إدارة هذه الالتهابات. ومع ذلك، لا يزال هناك جدل قائم حول استخدام العلاج بالأكسجين عالي الضغط في علاج التهابات الأنسجة الرخوة النخرية بسبب نقص الدراسات المستقبلية المضبوطة.تشير الأدلة إلى أنه قد يكون مرتبطًا بتحسن معدلات البقاء على قيد الحياة والحفاظ على الأعضاء لدى مرضى التهاب الأنسجة الرخوة الناخرةأشارت دراسة استرجاعية إلى انخفاض كبير في معدلات الوفيات بين مرضى التهاب الأنسجة الرخوة الناخرة الذين يتلقون العلاج بالأكسجين عالي الضغط.
1.3 عدوى موقع الجراحة
يمكن تصنيف عدوى مواقع الجراحة بناءً على الموقع التشريحي للعدوى، وقد تنشأ عن مسببات أمراض متنوعة، بما في ذلك البكتيريا الهوائية واللاهوائية. وعلى الرغم من التقدم المحرز في تدابير مكافحة العدوى، مثل تقنيات التعقيم، واستخدام المضادات الحيوية الوقائية، وتحسين الممارسات الجراحية، إلا أن عدوى مواقع الجراحة لا تزال تشكل من المضاعفات المستمرة.
أجرت إحدى الدراسات الهامة مراجعةً لفعالية العلاج بالأكسجين عالي الضغط في الوقاية من عدوى مواقع الجراحة العميقة في جراحة الجنف العصبي العضلي. قد يُسهم العلاج بالأكسجين عالي الضغط قبل الجراحة في تقليل حدوث عدوى مواقع الجراحة بشكل ملحوظ، كما يُسهّل التئام الجروح. يُهيئ هذا العلاج غير الجراحي بيئةً ترتفع فيها مستويات الأكسجين في أنسجة الجرح، وهو ما يرتبط بتأثيره المؤكسد في القضاء على مسببات الأمراض. إضافةً إلى ذلك، يُعالج انخفاض مستويات الدم والأكسجين الذي يُسهم في تطور عدوى مواقع الجراحة. وإلى جانب استراتيجيات مكافحة العدوى الأخرى، يُوصى بالعلاج بالأكسجين عالي الضغط، لا سيما في الجراحات النظيفة الملوثة، مثل جراحات القولون والمستقيم.
1.4 الحروق
الحروق هي إصابات ناتجة عن الحرارة الشديدة أو التيار الكهربائي أو المواد الكيميائية أو الإشعاع، وقد تُسبب معدلات عالية من المراضة والوفيات. يُعد العلاج بالأكسجين عالي الضغط مفيدًا في علاج الحروق عن طريق زيادة مستويات الأكسجين في الأنسجة المتضررة. بينما تُظهر الدراسات على الحيوانات والدراسات السريرية نتائج متباينة فيما يتعلق بهذا الأمر.فعالية العلاج بالأكسجين عالي الضغط في علاج الحروقأشارت دراسة شملت 125 مريضًا بالحروق إلى أن العلاج بالأكسجين عالي الضغط لم يُظهر تأثيرًا يُذكر على معدلات الوفيات أو عدد العمليات الجراحية، ولكنه قلل من متوسط فترة الشفاء (19.7 يومًا مقارنةً بـ 43.8 يومًا). ويمكن أن يُسهم دمج العلاج بالأكسجين عالي الضغط مع الإدارة الشاملة للحروق في السيطرة الفعّالة على الإنتان لدى مرضى الحروق، مما يؤدي إلى تقصير فترة الشفاء وتقليل الحاجة إلى السوائل. ومع ذلك، لا تزال هناك حاجة إلى مزيد من الأبحاث المستقبلية واسعة النطاق لتأكيد دور العلاج بالأكسجين عالي الضغط في علاج الحروق الشديدة.
1.5 التهاب العظم والنقي
التهاب العظم والنقي هو عدوى تصيب العظم أو نخاع العظم، وغالبًا ما تسببها مسببات الأمراض البكتيرية. يُعدّ علاج التهاب العظم والنقي صعبًا نظرًا لضعف التروية الدموية للعظام ومحدودية اختراق المضادات الحيوية لنخاع العظم. يتميز التهاب العظم والنقي المزمن باستمرار وجود مسببات الأمراض، والتهاب خفيف، وتكوّن نسيج عظمي نخر. أما التهاب العظم والنقي المقاوم للعلاج، فيشير إلى عدوى العظام المزمنة التي تستمر أو تتكرر رغم تلقي العلاج المناسب.
أظهرت الدراسات أن العلاج بالأكسجين عالي الضغط يُحسّن بشكل ملحوظ مستويات الأكسجين في أنسجة العظام المصابة. وتشير العديد من الدراسات السريرية والدراسات الجماعية إلى أن هذا العلاج يُحسّن النتائج السريرية لمرضى التهاب العظم والنقي. ويبدو أنه يعمل من خلال آليات متعددة، تشمل تعزيز النشاط الأيضي، وكبح مسببات الأمراض البكتيرية، وتعزيز فعالية المضادات الحيوية، وتقليل الالتهاب، وتعزيز الشفاء.العمليات. بعد العلاج بالأكسجين عالي الضغط، تظهر علامات كبت العدوى لدى 60% إلى 85% من المرضى الذين يعانون من التهاب العظم والنقي المزمن والمقاوم للعلاج.
1.6 العدوى الفطرية
على الصعيد العالمي، يعاني أكثر من ثلاثة ملايين شخص من عدوى فطرية مزمنة أو غازية، مما يؤدي إلى أكثر من 600 ألف حالة وفاة سنويًا. غالبًا ما تتأثر نتائج علاج العدوى الفطرية سلبًا بعوامل مثل ضعف المناعة، والأمراض الكامنة، وخصائص ضراوة العامل الممرض. يُعد العلاج بالأكسجين عالي الضغط خيارًا علاجيًا واعدًا في حالات العدوى الفطرية الشديدة نظرًا لسلامته وطبيعته غير الغازية. تشير الدراسات إلى أن العلاج بالأكسجين عالي الضغط قد يكون فعالًا ضد مسببات الأمراض الفطرية مثل فطر الرشاشيات (Aspergillus) وبكتيريا السل (Mycobacterium tuberculosis).
يعزز العلاج بالأكسجين عالي الضغط التأثيرات المضادة للفطريات عن طريق تثبيط تكوين الأغشية الحيوية لفطر الرشاشيات، مع ملاحظة زيادة في الفعالية لدى السلالات التي تفتقر إلى جينات إنزيم ديسموتاز الفائق (SOD). تشكل ظروف نقص الأكسجين أثناء العدوى الفطرية تحديات أمام توصيل الأدوية المضادة للفطريات، مما يجعل زيادة مستويات الأكسجين الناتجة عن العلاج بالأكسجين عالي الضغط تدخلاً مفيداً محتملاً، على الرغم من الحاجة إلى مزيد من البحث.
الخصائص المضادة للميكروبات للعلاج بالأكسجين عالي الضغط
تُحفز البيئة الغنية بالأكسجين التي يوفرها العلاج بالأكسجين عالي الضغط تغييرات فسيولوجية وكيميائية حيوية تُعزز الخصائص المضادة للبكتيريا، مما يجعله علاجًا مساعدًا فعالًا للعدوى. يُظهر العلاج بالأكسجين عالي الضغط تأثيرات ملحوظة ضد البكتيريا الهوائية، وخاصة اللاهوائية، من خلال آليات مثل النشاط القاتل للبكتيريا المباشر، وتعزيز الاستجابات المناعية، والتأثيرات التآزرية مع عوامل مضادة للميكروبات محددة.
2.1 التأثيرات المضادة للبكتيريا المباشرة للعلاج بالأكسجين عالي الضغط
يُعزى التأثير المضاد للبكتيريا المباشر للعلاج بالأكسجين عالي الضغط إلى حد كبير إلى توليد أنواع الأكسجين التفاعلية (ROS)، والتي تشمل أنيونات فوق الأكسيد، وبيروكسيد الهيدروجين، وجذور الهيدروكسيل، وأيونات الهيدروكسيل - وكلها تنشأ أثناء عملية التمثيل الغذائي الخلوي.
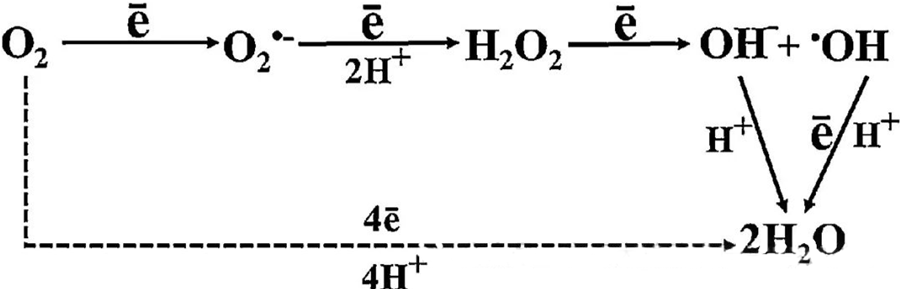
يُعدّ التفاعل بين الأكسجين (O₂) ومكونات الخلية أساسيًا لفهم كيفية تكوّن أنواع الأكسجين التفاعلية (ROS) داخل الخلايا. في ظل ظروف معينة تُعرف بالإجهاد التأكسدي، يختل التوازن بين تكوّن أنواع الأكسجين التفاعلية وتحللها، مما يؤدي إلى ارتفاع مستوياتها في الخلايا. يُحفّز إنزيم ديسموتاز الفائق الأكسيد إنتاج الأكسيد الفائق (O₂⁻)، الذي يحوّله بدوره إلى بيروكسيد الهيدروجين (H₂O₂). ويتضاعف هذا التحوّل بفعل تفاعل فنتون، الذي يؤكسد أيونات الحديد الثنائي (Fe²⁺) لتوليد جذور الهيدروكسيل (·OH) وأيونات الحديد الثلاثي (Fe³⁺)، مما يُطلق سلسلة تفاعلات أكسدة واختزال ضارة تُؤدي إلى تكوّن أنواع الأكسجين التفاعلية وتلف الخلايا.
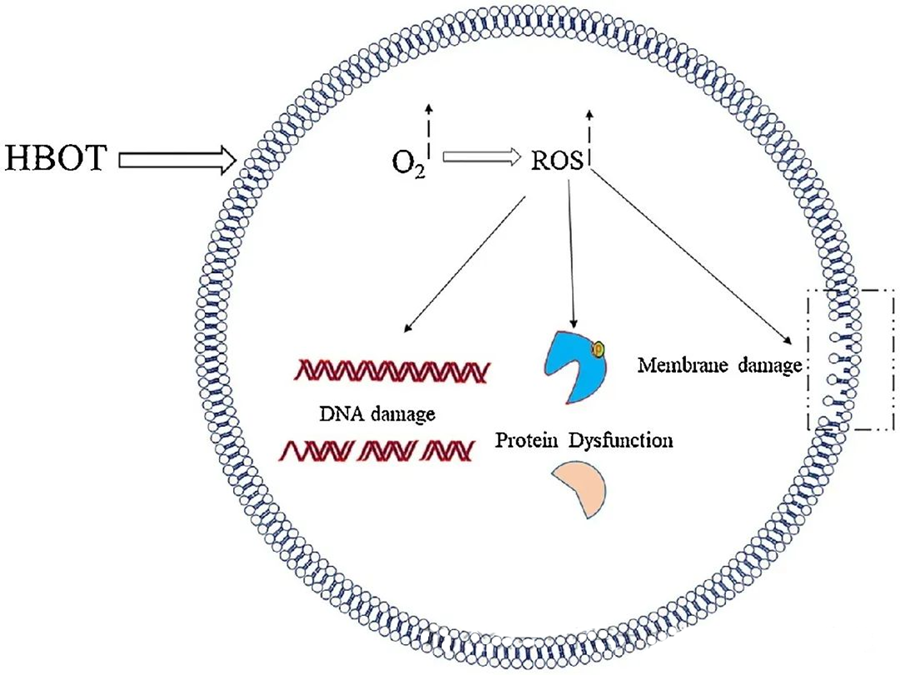
تستهدف التأثيرات السامة لأنواع الأكسجين التفاعلية مكونات خلوية حيوية مثل الحمض النووي (DNA) والحمض النووي الريبوزي (RNA) والبروتينات والدهون. ومن الجدير بالذكر أن الحمض النووي (DNA) يُعد هدفًا رئيسيًا للسمية الخلوية التي يُسببها بيروكسيد الهيدروجين (H₂O₂)، حيث يُعطّل بنية الديوكسي ريبوز ويُتلف تركيب القواعد النيتروجينية. ويمتد الضرر الفيزيائي الناجم عن أنواع الأكسجين التفاعلية إلى بنية الحمض النووي الحلزونية، وقد ينتج ذلك عن بيروكسدة الدهون التي تُحفزها هذه الأنواع. وهذا يُؤكد على العواقب الوخيمة لارتفاع مستويات أنواع الأكسجين التفاعلية داخل الأنظمة البيولوجية.
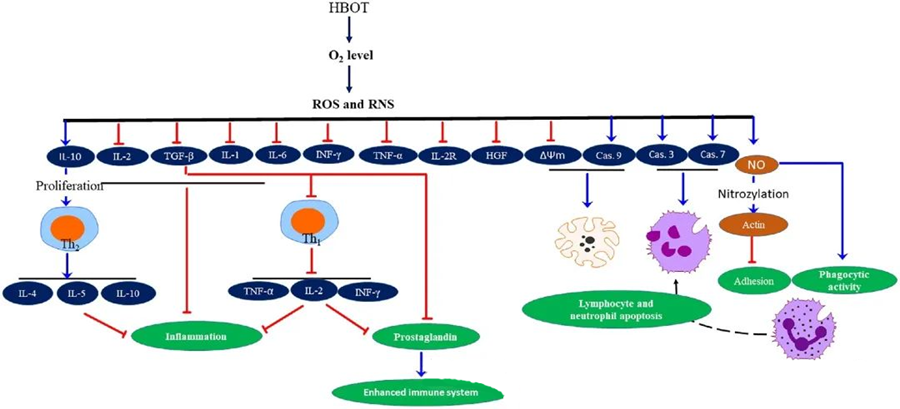
التأثير المضاد للميكروبات لأنواع الأكسجين التفاعلية
تلعب أنواع الأكسجين التفاعلية دورًا حيويًا في تثبيط نمو الميكروبات، كما يتضح من خلال توليدها الناتج عن العلاج بالأكسجين عالي الضغط. تستهدف التأثيرات السامة لأنواع الأكسجين التفاعلية مكونات الخلية مباشرةً، مثل الحمض النووي والبروتينات والدهون. يمكن أن تؤدي التركيزات العالية من أنواع الأكسجين النشطة إلى إتلاف الدهون مباشرةً، مما يؤدي إلى بيروكسدة الدهون. تُضعف هذه العملية سلامة أغشية الخلايا، وبالتالي وظائف المستقبلات والبروتينات المرتبطة بالغشاء.
علاوة على ذلك، تخضع البروتينات، التي تُعدّ أهدافًا جزيئية مهمة لأنواع الأكسجين التفاعلية، لتعديلات تأكسدية محددة في بقايا أحماض أمينية مختلفة مثل السيستين والميثيونين والتيروسين والفينيل ألانين والتريبتوفان. على سبيل المثال، ثبت أن العلاج بالأكسجين عالي الضغط يحفز تغيرات تأكسدية في العديد من البروتينات في بكتيريا الإشريكية القولونية، بما في ذلك عامل الاستطالة G وDnaK، مما يؤثر على وظائفها الخلوية.
تعزيز المناعة من خلال العلاج بالأكسجين عالي الضغط
الخصائص المضادة للالتهابات للعلاج بالأكسجين عالي الضغطتم توثيق هذه النتائج، مما يثبت أهميتها البالغة في تخفيف تلف الأنسجة وكبح تطور العدوى. يؤثر العلاج بالأكسجين عالي الضغط بشكل كبير على التعبير عن السيتوكينات وغيرها من منظمات الالتهاب، مما يؤثر على الاستجابة المناعية. وقد لاحظت أنظمة تجريبية مختلفة تغيرات متباينة في التعبير الجيني وإنتاج البروتين بعد العلاج بالأكسجين عالي الضغط، والتي إما تزيد أو تقلل من عوامل النمو والسيتوكينات.
أثناء عملية العلاج بالأكسجين عالي الضغط، يؤدي ارتفاع مستويات الأكسجين إلى تحفيز سلسلة من الاستجابات الخلوية، مثل تثبيط إطلاق الوسائط الالتهابية وتعزيز موت الخلايا اللمفاوية والعدلات. وتساهم هذه الإجراءات مجتمعةً في تعزيز آليات الجهاز المناعي المضادة للميكروبات، مما يُسهّل شفاء العدوى.
علاوة على ذلك، تشير الدراسات إلى أن زيادة مستويات الأكسجين أثناء العلاج بالأكسجين عالي الضغط قد تُقلل من التعبير عن السيتوكينات المُحفزة للالتهاب، بما في ذلك إنترفيرون غاما (IFN-γ) وإنترلوكين-1 (IL-1) وإنترلوكين-6 (IL-6). وتشمل هذه التغييرات أيضًا خفض نسبة الخلايا التائية المساعدة (CD4) إلى الخلايا التائية السامة (CD8) وتعديل مستقبلات ذائبة أخرى، مما يؤدي في النهاية إلى رفع مستويات إنترلوكين-10 (IL-10)، وهو أمر بالغ الأهمية لمكافحة الالتهاب وتعزيز الشفاء.
تتشابك الأنشطة المضادة للميكروبات للعلاج بالأكسجين عالي الضغط مع آليات بيولوجية معقدة. وقد أشارت التقارير إلى أن كلاً من الأكسيد الفائق والضغط المرتفع يعززان، بشكل غير متسق، النشاط المضاد للبكتيريا وموت الخلايا المتعادلة الناتج عن العلاج بالأكسجين عالي الضغط. بعد العلاج، يؤدي الارتفاع الملحوظ في مستويات الأكسجين إلى تعزيز القدرات القاتلة للبكتيريا لدى الخلايا المتعادلة، وهي عنصر أساسي في الاستجابة المناعية. علاوة على ذلك، يثبط العلاج بالأكسجين عالي الضغط التصاق الخلايا المتعادلة، والذي يتوسطه تفاعل مستقبلات بيتا-إنتغرين على سطح الخلايا المتعادلة مع جزيئات الالتصاق بين الخلايا (ICAM) على الخلايا البطانية. كما يثبط العلاج بالأكسجين عالي الضغط نشاط مستقبل بيتا-2 إنتغرين (Mac-1، CD11b/CD18) على سطح الخلايا المتعادلة من خلال عملية تتوسطها أكسيد النيتريك (NO)، مما يساهم في هجرة الخلايا المتعادلة إلى موقع العدوى.
يُعدّ إعادة تنظيم الهيكل الخلوي بدقة أمرًا ضروريًا لكي تتمكن العدلات من ابتلاع مسببات الأمراض بفعالية. وقد ثبت أن إضافة مجموعة النترزة إلى الأكتين تحفز بلمرة الأكتين، مما قد يُسهّل نشاط البلعمة لدى العدلات بعد المعالجة المسبقة بالأكسجين عالي الضغط. علاوة على ذلك، يُعزز الأكسجين عالي الضغط موت الخلايا المبرمج في خطوط الخلايا التائية البشرية عبر مسارات الميتوكوندريا، مع الإبلاغ عن تسارع موت الخلايا اللمفاوية بعد العلاج بالأكسجين عالي الضغط. وقد أظهر تثبيط كاسبيز-9 - دون التأثير على كاسبيز-8 - التأثيرات المناعية المعدلة للأكسجين عالي الضغط.
التأثيرات التآزرية للعلاج بالأكسجين عالي الضغط مع العوامل المضادة للميكروبات
في التطبيقات السريرية، يُستخدم العلاج بالأكسجين عالي الضغط (HBOT) بشكل متكرر بالتزامن مع المضادات الحيوية لمكافحة العدوى بفعالية. ويمكن أن تؤثر حالة فرط الأكسجين التي يتم الوصول إليها أثناء العلاج بالأكسجين عالي الضغط على فعالية بعض المضادات الحيوية. وتشير الأبحاث إلى أن بعض الأدوية المبيدة للبكتيريا، مثل البيتا لاكتام والفلوروكينولونات والأمينوغليكوزيدات، لا تعمل فقط من خلال آلياتها الذاتية، بل تعتمد جزئيًا أيضًا على عملية التمثيل الغذائي الهوائي للبكتيريا. ولذلك، يُعد وجود الأكسجين والخصائص الأيضية لمسببات الأمراض أمرًا بالغ الأهمية عند تقييم التأثيرات العلاجية للمضادات الحيوية.
أظهرت أدلة قوية أن انخفاض مستويات الأكسجين يزيد من مقاومة بكتيريا الزائفة الزنجارية لبيبراسيلين/تازوباكتام، وأن بيئة نقص الأكسجين تُسهم أيضًا في زيادة مقاومة بكتيريا الأمعاء الكلوكية للأزيثروميسين. في المقابل، قد تُعزز بعض حالات نقص الأكسجين حساسية البكتيريا لمضادات التتراسيكلين. يُعد العلاج بالأكسجين عالي الضغط طريقة علاجية مساعدة فعّالة، إذ يُحفز عملية التمثيل الغذائي الهوائي ويُعيد أكسجة الأنسجة المصابة بنقص الأكسجين، مما يزيد لاحقًا من حساسية مسببات الأمراض للمضادات الحيوية.
في الدراسات ما قبل السريرية، أدى الجمع بين العلاج بالأكسجين عالي الضغط (HBOT) - الذي يُعطى مرتين يوميًا لمدة 8 ساعات عند ضغط 280 كيلو باسكال - مع التوبراميسين (20 ملغم/كغم/يوم) إلى انخفاض ملحوظ في الحمل البكتيري في التهاب الشغاف المعدي الناتج عن المكورات العنقودية الذهبية. وهذا يُظهر إمكانية استخدام العلاج بالأكسجين عالي الضغط كعلاج مساعد. وكشفت دراسات أخرى أن العلاج بالأكسجين عالي الضغط، عند درجة حرارة 37 درجة مئوية وضغط 3 ضغط جوي مطلق لمدة 5 ساعات، عزز بشكل ملحوظ تأثير الإيميبينيم ضد الزائفة الزنجارية المصابة بالخلايا البلعمية. بالإضافة إلى ذلك، وُجد أن الجمع بين العلاج بالأكسجين عالي الضغط والسيفازولين أكثر فعالية في علاج التهاب العظم والنقي الناتج عن المكورات العنقودية الذهبية في النماذج الحيوانية مقارنةً باستخدام السيفازولين وحده.
يزيد العلاج بالأكسجين عالي الضغط بشكل ملحوظ من فعالية السيبروفلوكساسين في قتل الأغشية الحيوية لبكتيريا الزائفة الزنجارية، خاصةً بعد 90 دقيقة من التعرض. ويعزى هذا التحسن إلى تكوين أنواع الأكسجين التفاعلية الداخلية، ويُظهر حساسية متزايدة في الطفرات التي تعاني من نقص في إنزيم البيروكسيداز.
في نماذج التهاب الجنبة الناجم عن المكورات العنقودية الذهبية المقاومة للميثيسيلين (MRSA)، أظهر التأثير التآزري للفانكومايسين والتيكوبلانين واللينزوليد مع العلاج بالأكسجين عالي الضغط فعاليةً متزايدةً بشكل ملحوظ ضد MRSA. وقد أظهر الميترونيدازول، وهو مضاد حيوي يُستخدم على نطاق واسع في علاج العدوى اللاهوائية الشديدة والعدوى متعددة الميكروبات، مثل عدوى القدم السكرية وعدوى مواقع الجراحة، فعاليةً مضادةً للميكروبات أعلى في الظروف اللاهوائية. وتستدعي الحاجة إجراء دراسات مستقبلية لاستكشاف التأثيرات المضادة للبكتيريا التآزرية للعلاج بالأكسجين عالي الضغط مع الميترونيدازول في كل من التجارب على الحيوانات الحية وفي المختبر.
فعالية العلاج بالأكسجين عالي الضغط كمضاد للميكروبات على البكتيريا المقاومة
مع تطور وانتشار السلالات المقاومة، تفقد المضادات الحيوية التقليدية فعاليتها بمرور الوقت. علاوة على ذلك، قد يكون العلاج بالأكسجين عالي الضغط ضروريًا في علاج ومنع العدوى التي تسببها مسببات الأمراض المقاومة للأدوية المتعددة، حيث يُعد استراتيجية حاسمة عند فشل العلاجات بالمضادات الحيوية. وقد أفادت دراسات عديدة بالتأثيرات القاتلة للبكتيريا الكبيرة للعلاج بالأكسجين عالي الضغط على البكتيريا المقاومة ذات الأهمية السريرية. على سبيل المثال، أدت جلسة علاج بالأكسجين عالي الضغط لمدة 90 دقيقة عند ضغط جوي 2 إلى تقليل نمو المكورات العنقودية الذهبية المقاومة للميثيسيلين بشكل كبير. بالإضافة إلى ذلك، في نماذج النسبة، عزز العلاج بالأكسجين عالي الضغط التأثيرات المضادة للبكتيريا لمختلف المضادات الحيوية ضد عدوى المكورات العنقودية الذهبية المقاومة للميثيسيلين. وقد أكدت التقارير أن العلاج بالأكسجين عالي الضغط فعال في علاج التهاب العظم والنقي الناجم عن بكتيريا كليبسيلا الرئوية المنتجة لإنزيم OXA-48 دون الحاجة إلى أي مضادات حيوية إضافية.
باختصار، يُمثل العلاج بالأكسجين عالي الضغط نهجًا متعدد الجوانب لمكافحة العدوى، إذ يُعزز الاستجابة المناعية ويُضاعف فعالية المضادات الحيوية المتوفرة. وبفضل البحث والتطوير الشاملين، يُمكن لهذا العلاج أن يُخفف من آثار مقاومة المضادات الحيوية، مما يُعطي أملًا في المعركة المستمرة ضد العدوى البكتيرية.
تاريخ النشر: 28 فبراير 2025

